0
新航道官方在线客服


锦秋A-Level学院作为隶属于新航道国际教育集团的高端子品牌,专为有志于申请英国G5及英澳高校的中学生设计,紧抓中国学生理科优势,进行课程组合化。开设数学、物理、化学、生物、经济学、会计学等课程,帮助学生以优异成绩申请更好的大学。
A-Level化学中的有机部分,是个名副其实的难点,因为有大量的反应和机制需要理解和记忆,但是当大家认真学完,回过头来就会发现也就那么回事。
本篇文章就将为大家讲解有机化学的个部分:苯环(benzene)
首先大家需要知道两个概念
芳烃(arene):Organic hydrocarbons containing one or more benzene rings.
芳基化合物(aryl compound):compounds of benzene.
这里的aryl是一个官能团,芳基,即苯环失去电子后形成的基团。
苯环的结构
对于苯环的结构化学家们早期有一些猜测,其中的是十九世纪德国化学家凯库勒的猜想,他猜的结构其实也算不错了,只是细节不太对。他提出了一个六边形的模型,包含三个碳碳双键。但是后来呢,随着化学分析技术的发展,人们发现苯环的结构是个平面,完全对称的正六边形。这就和凯库勒的观点有出入了,凯库勒说有双键,如果真的有双键,那么这个六边形不应该是完全对称的,因为双键之间的作用力比单键强,所以多少会distort一下这个六边形。其次,化学家们发现苯环不会发生加成反应,这也说明了苯环没有双键。那么这个比单键强又不是双键的键什么呢?我们先来看看碳原子的核外电子排布。
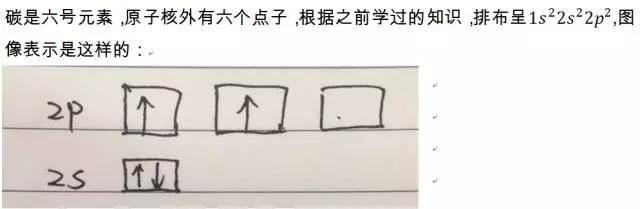
在苯环中呢,碳原子会发生sp2杂化(hybridize),变成这样:

✪简而言之,就是2s轨道上的一个电子跑到了2p压层的一个空轨道上,这样,四个电子就在四个不同的轨道上了。这个过程就叫做sp2杂化。
杂化过后的四个电子呢,各司其职。一个电子和隔壁的碳原子成键;一个电子和另一个相邻的碳原子成键;一个电子和一个氢原子成键。注意以上说的都是sigma bonds( bonds),也就是存在于s轨道之间,以及两个p轨道之间的键。大家还记得p亚层是有三个轨道的,其中的两个可以成sigma键,另一个则会形成pi键( bond),这是因为p层三个轨道的排布方式。所以这些碳原子外的第四个电子,也就是p亚层剩下的最后一个电子,会形成一个大pi键,which are not localized between pairs of carbon atoms. They spread overall six carbon atoms in the hexagonal ring. 这也是苯环内的碳碳键能介于单键和双键之间的原因。
✪附上一张助于大家理解大pi键的苯环结构图:
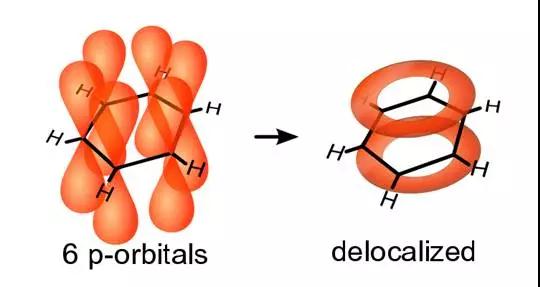
大家会遇到关于苯环结构的考题,具体的回答方式就参考上一段我的解释,包括杂化,和pi键是如何形成的,怎么分布的。
苯的化合物的命名
如果苯环连了一个卤素原子,就叫某某benzene。比如氯原子,就叫chlorobenzene;
如果苯环连了硝基(-NO2),就叫nitrobenzene;
如果苯环连了一个-OH,这就是我们以后要讲的另一种化合物,phenol,苯酚。
如果连了一个氨基(-NH2),注意和硝基区分,就叫phenylamine。
新航道锦秋A-Level项目针对不同学员的不同层次的学习需求,有针对性的制定课程计划和教学方式:班课和一对一混合学习,科学合理,符合中国学生学习习惯,针对不同年级和基础,选择更丰富。同时配备海量国际背景的教师和专业助教团队,双管齐下,奠定每一位学员的G5之路。
| 大学名称 | QS排名 |
|---|---|
| 麻省理工学院 | 1 |
| 剑桥大学 | 3 |
| 斯坦福大学 | 3 |
| 牛津大学 | 2 |
| 哈佛大学 | 5 |
| 加州理工学院 | 6 |
| 帝国理工学院 | 7 |
| 伦敦大学学院 | 8 |
| 苏黎世联邦理工大学 | 8 |
| 芝加哥大学 | 10 |
| 新加坡国立大学 | 11 |
| 宾夕法尼亚大学 | 13 |
| 洛桑联邦理工学院 | 14 |
网络优惠
预约试听
A-Level
雅思
留学咨询
留学规划